不整脈のより適切な管理のために
監修・症例提供:慶應義塾大学医学部 循環器内科 専任講師 遠藤仁 先生
紹介の経緯
| 患者さんの年齢・性別 | 80代、男性 |
|---|---|
| 紹介元 | 都内の総合病院の循環器科 |
| 紹介理由 | 心アミロイドーシスの精査加療目的 |
| 検査所見 | 心房細動のアブレーション手術のために入院した際の術前検査において、心電図で低電位、心エコーで拡張障害と心室中隔肥大(IVST12~13mm)が確認された。アブレーションの際、右室の2ヵ所から生検を実施。コンゴーレッド陽性でアミロイド沈着を確認。 |
| 既往歴 | 特になし |
紹介後のスクリーニング検査
心エコー:中等度の僧帽弁閉鎖不全を認め、両心房とも拡大していた。左室肥大はIVST12~13mm程度で、左室収縮は左室駆出率(LVEF)51%程度で保たれていた。
心エコー画像
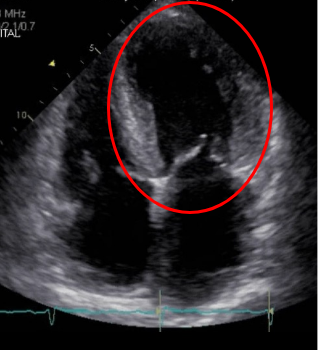
脚注:左室肥大(図中赤〇)が確認できる。
診断所見
シンチグラフィ:99mTcピロリン酸シンチグラフィでGrade 3を確認し、心アミロイドーシスに合致する所見であった。
シンチグラフィ(3時間後撮影)の造影画像
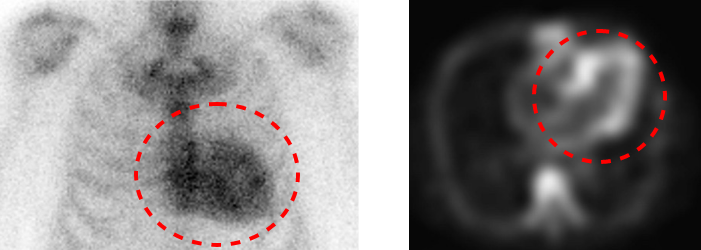
脚注:PYPシンチグラフィで、Grade 3の集積像を認めた。Planar像(左)、SPECT像(右)。
血液検査:M蛋白の確認を行ったところ、確認されなかった。
生検:他院の心筋生検検体を送っていただき、当院でコンゴーレッド染色と免疫染色を行った結果、ATTRアミロイドーシスと確定診断された。
染色後の心筋組織画像
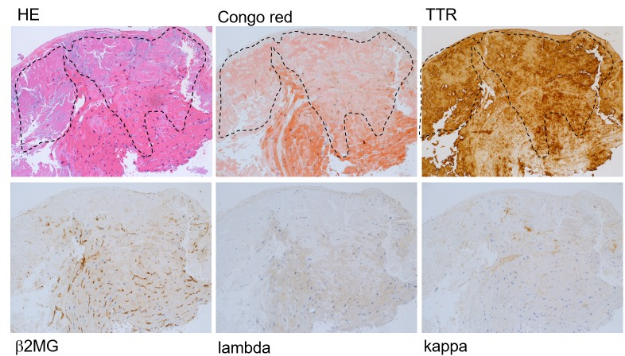
脚注:組織に沈着しているアミロイドが確認でき、一致してTTRが陽性を示す(点線内)。免疫染色は頻度の高いアミロイドーシスの病型に関してパネル染色を行う。
フォローアップ頻度と検査内容
フォローアップ頻度:3ヵ月程度の間隔で診ており、処方は98日分。
フォローアップ時の注意事項:特に心エコーを重視。EFについては50%で経時的な変化は認めないが、当初-15%ほどあったGlobal Longitudinal Strain(GLS)は現在-12%に低下している。このように、EFの変化はなくても、GLSに悪化がみられるケースはよく経験する。
現在の病状
目立った心不全症状もなく、落ち着いた経過を辿っている。
監修医コメント
カテーテルアブレーションの際に、心筋生検を同時に行える場合があります。一方で、そういった機会を逃してしまうと、再度心筋生検のためだけに侵襲的なカテーテル検査の調整が必要になってしまい、患者さん及び連携する医療スタッフの負担となってしまいます。事前にスクリーニングを行い、アミロイドーシスの確証がある程度得られている場合、積極的な心筋生検により早期発見に繋がる可能性が高まります。
心エコー
心エコー画像
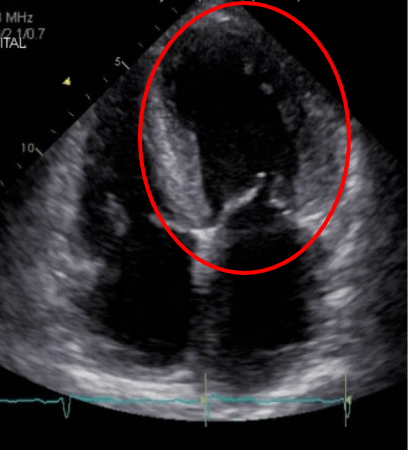
脚注:左室肥大(図中赤〇)が確認できる。
心電図
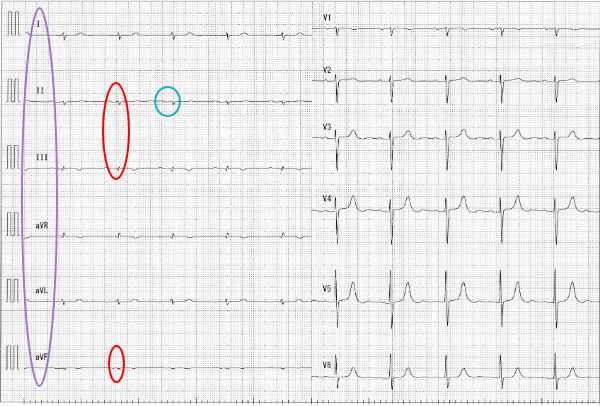
脚注:洞調律、紫:四肢誘導低電位、赤:左脚前枝ブロック、青:1度房室ブロック
シンチグラフィ
シンチグラフィ(3時間後撮影)の造影画像
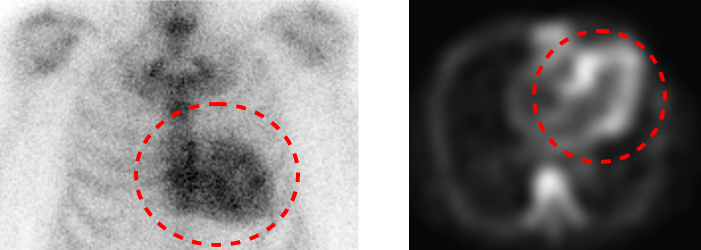
脚注:PYPシンチグラフィで、Grade 3の集積像を認めた。Planar像(左)、SPECT像(右)。
1. Atrial fibrillation in amyloidotic cardiomyopathy: prevalence, incidence, risk factors and prognostic role(海外データ)
Longhi S, et al. Amyloid. 2015; 22(3): 147-155.
心房細動(AF)は心アミロイドーシスの合併症の1つであるが、合併症としての正確な病態や予後の特徴は得られていない。そこで、軽鎖型(AL)、遺伝性トランスサイレチン(ATTRv)及び野生型トランスサイレチン(ATTRwt)の各心アミロイドーシスにおける心房細動の有病率、発生率、危険因子及び予後を評価することを目的とした。
単一施設の心アミロイドーシス患者262例(AL123例、ATTRv94例、ATTRwt45例)の後ろ向きに解析したところ、AF有病率はALで8.9%、ATTRvで10.6%、ATTRwtで37.8%とグループ間で有意差が認められた(p<0.0001、Studentのt検定)。また、追跡期間中央値1.2年の間に11例がAFを発症した(2.1%人/年)。AF発症の危険因子として、年齢、心不全(HF)、LVEF、腎障害、左房径、右房圧が報告された。また、AFによる予後への影響については、本研究では認められなかった。
