監修:高知大学医学部 老年病・循環器内科学講座 教授 北岡裕章 先生
1.TTRとATTR-CM
1) TTRとは?
プレアルブミンとしても知られるTTRは、人体にとって重要な役割を果たしています1,2)。
- 甲状腺ホルモンであるサイロキシンや、レチノール結合蛋白(RBP)を介したレチノール(ビタミンA)の輸送を担う。
- 神経の保護、記憶や認知機能維持、脳虚血からの保護。
2) ATTR-CMとは?
トランスサイレチン型心アミロイドーシス(ATTR-CM:Transthyretin Amyloid Cardiomyopathy)は、TTR四量体由来のトランスサイレチンアミロイド(ATTR:Transthyretin
Amyloid)が心筋組織に沈着することで引き起こされます3)。
ATTR-CMの診断数は近年増加していますが4,5)、未診断患者は相当数いることが推測されます。
3) ATTR-CMの予後と入院頻度(未治療の場合)
ATTR-CMは、進行性かつ致死性の疾患です。本邦における野生型トランスサイレチンアミロイドーシス(ATTRwtアミロイドーシス)患者の予後の研究で、未治療の場合の全生存期間の中央値は約3.8年であったと報告されています6)。一般に、入院は予後不良の予測因子であることが知られています7)。ATTR-CMでは、診断後未治療の場合、1年間で60%以上の患者が1回以上の入院を経験したと報告されています8)。
そのため、ATTR-CMでは入院の抑制を目指した治療戦略が求められます。それにもかかわらず、認知度の低さ等から、診断の遅れが報告されています9)。42%の症例では、心症状を呈してから4年以上の診断の遅れがあったという報告もあります(海外データ)8)。
2.TTR不安定化がATTR-CMの発症機序
加齢や遺伝子変異によってTTR四量体が不安定化することが、ATTR-CM発症の根本原因です3,10)。
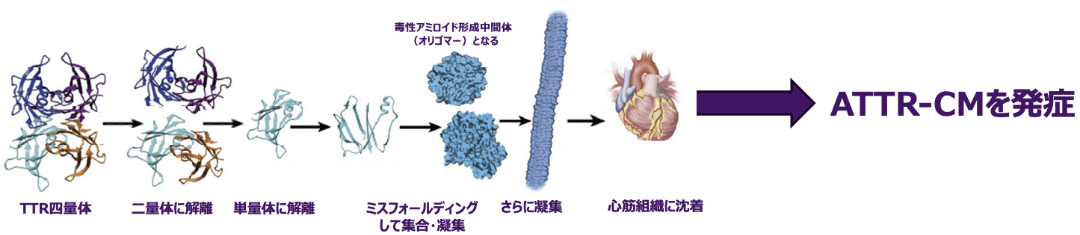
TTRは通常、四量体を形成していますが、構造の不安定化により、単量体へ解離します。単量体はミスフォールディングを起こし、集合・凝集してアミロイドを形成します10)。ATTR-CMでは、アミロイドが心臓のあらゆる構造に浸潤し11)、心臓壁の肥厚や拡張障害・収縮障害・伝導障害等を引き起こします12)。
また、アミロイド由来の心不全は心筋リモデリングよりも、主に間質へのアミロイドの浸潤によって引き起こされるため、β遮断薬の使用は有益ではないとされ、ACE阻害薬やARBといった従来の心不全治療薬についても、忍容性が低く、症状の悪化を招くリスクがあるとされています13)。
ATTR-CMは、TTRが不安定化する要因により2つのサブタイプ(野生型、変異型)にわけられ、それぞれ異なった特徴を有しています。2つのサブタイプはそれぞれ、加齢による変化(野生型)やTTR遺伝子の変異(変異型)等により、TTR四量体を不安定化する構造変化を引き起こす可能性があります3)。
ATTR-CM発症の流れ
1) TTR安定化と症状・予後の関連
1-1) 血漿TTRレベルと心不全発症リスク
血漿TTR レベルと心不全発症との関連を検討した研究で、血漿TTR 低値群*、中間群*、高値群*で比較したところ、低値群では他2群より心不全の発症リスクが有意に高いことが報告されました(p<0.001、Gray検定、海外データ)14)。
- 血漿TTR レベルが5パーセンタイル以下を低値群、5-95パーセンタイルを中間群、95パーセンタイル以上を高値群と定義している。
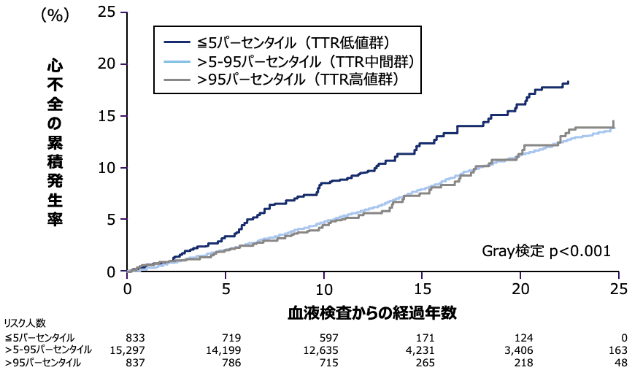
Reproduced with permission from [JAMA Cardiol. 2021. 6(3): 258-266].Copyright © 2021 American Medical Association. All rights reserved, including those for text and data mining, AI training, and similar technologies.
対象:2つのコホート研究に含まれたデンマークの一般母集団16,967例(Copenhagen General Population Study:9,582例、Copenhagen City Heart Study:7,385例)方法:全国市民登録システムを使用して自記式質問票、身体検査、及び血液検査からデータを取得し、TTRのパーセンタイルによって層別化された血液検査からの経過年数の関数としての心不全の累積発生率を算出した。
解析:層別化は血中のTTR濃度で行われ、2つのコホート研究の集団毎に≦5パーセンタイル(TTR低値群)、>5-95パーセンタイル(TTR中間群)、>95パーセンタイル(TTR高値群)に分けられた*。血漿TTR濃度に最も関連するベースライン特性は95%CI正規化回帰係数によって特定され、ベースラインの血漿TTR濃度による心不全のハザード比はCox回帰によって計算した。また、競合イベントとして全死因死亡率を使用し、ノンパラメトリックなAalen-Johansen推定量を使用して、血液検査からの経過年数の関数として心不全の絶対確率を計算した。
リミテーション:高血圧や虚血性心疾患などの心不全の原因は特定できなかった。また、本研究ではサンプル数に限りがあるため2つのコホートにおいて異なるTTRの測定方法が使用され、白人のみを対象とした。
- Copenhagen General Population Study、 Copenhagen City Heart Studyについて、TTR低値群の濃度はそれぞれ7.0-19.0mg/dL、1.0-14.4mg/dL、TTR中間群の濃度はそれぞれ19.1-40.8mg/dL、14.5-38.0mg/dL、TTR高値群の濃度はそれぞれ40.9-77.7mg/dL、38.1-86.7mg/dLであった。
Greve AM, et al. JAMA Cardiol. 2021; 6(3) 258-266.
Kaplan-Meier解析(海外データ)
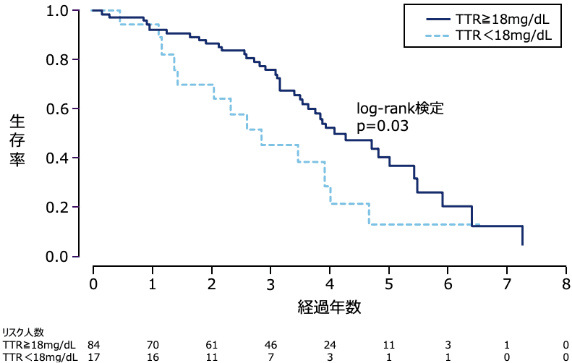
方法:追跡調査期間中に治療を受けなかった患者をベースラインのTTR閾値(18mg/dL)によって層別化し、生存率を比較した。
解析:追跡調査期間中に治療を受けなかった患者(n=101)を、ベースラインのTTR閾値18mg/dLによって層別化した。OS曲線はKaplan-Meier法で推定し、log-rank検定を用いて比較した。
リミテーション:比較的少人数の患者コホートでの検討のため、検出力は低かった。本研究では、心エコー、心臓MRI、核画像データ及びATTRwt-CM患者のモニタリングにおいて重要と考えられているNT-proBNP測定は行っていない。
Hanson JLS, et al. Circ Heart Fail. 2018; 11(2): e004000.
1-2) 血清TTRレベルと死亡リスク
野生型ATTR-CM(ATTRwt-CM)患者の血清TTRレベルと生存率との関連について、血清TTRを低値群*、高値群*で比較した研究では、血清TTR 低値群は高値群と比較し生存期間が短かったことが報告されました(HR:2.3、p=0.03、95%CI:1.2~4.2 、log-rank 検定、海外データ)15)。
- 血清TTR18mg/dLを閾値として、18mg/dL以上を高値群、18mg/dL未満を低値群と定義している。
2) 血中TTRレベルに関与するTTR遺伝子の変異
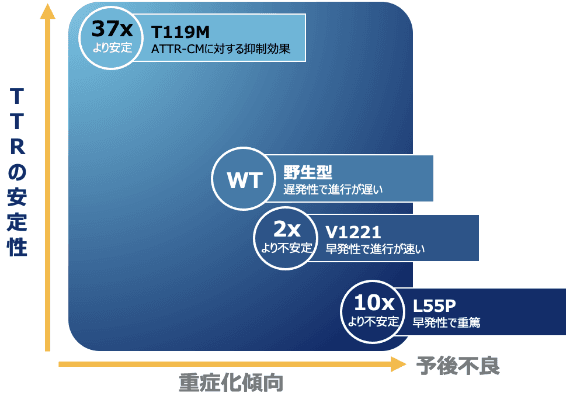
TTRにはV122I、T119M等の変異体があり、四量体の解離速度が速いもの(例:V122I、L55P)はアミロイド形成を促進し、解離速度が遅いもの(例:T119M)はアミロイド形成に抑制的に働きます16)。
同定された変異体の中でも、T119M変異によるTTR四量体の安定化は、本来構造の37倍に及びます16)。
T119Mは効果的に四量体の解離を妨げ、アミロイドの形成を防ぐのに役立つことが知られています16)。
T119M変異保持者は、非保持者と比較して、以下が報告されています。
- 血漿TTRレベルが高い(p=0.007、Mann-WhitneyのU検定、海外データ)17)
- 心血管疾患を含む血管疾患の発症リスクが30%減少(ハザード比0.7、p=0.03、95%CI:0.51~0.97、Cox比例ハザードモデル、海外データ)17)
Hammarström P. et al. Proc Natl Acad Sci USA. 2022; 99(Suppl 4): 16427-16432.
Hornstrup LS, et al. Arterioscler Thromb Vasc Biol. 2013; 33: 1441-1447.
以上のことから、TTRの安定化のレベルを高く保つことは、新たなアミロイドの集合・凝集を防ぎ、心症状の進行を遅らせることにつながります14-17)。
2)Vieira M, Saraiva MJ. Biomol Concepts. 2014; 5(1): 45-54.
3)Kittleson MM, et al. Circulation. 2020; 142(1): e7-e22.
[COI:著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]
4)Yamada T, et al. ESC Heart Failure. 2020; 7(5): 2829–2837.
5)Nativi-Nicolau J, et al. J Am Coll Cardiol CardioOnc. 2021; 3(4): 537–546.
[COI:著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受託している者が含まれる]
6)Ochi Y, et al. Circ Rep. 2020; 2(6): 314-321.
7)Setoguchi S, et al. Am Heart J.2007; 154(2): 260-266.
8)Lane T, et al. Circulation. 2019;140(1):16-26.
9)Rozenbaum MH, et al. Cardiol Ther. 2021; 10(1): 141-159.
[COI:著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]
11)Yilmaz, A et al. Clin Res Cardiol. 2021; 110(4): 479-506.
12)日本循環器学会.2020年版 心アミロイドーシス診療ガイドライン. https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2020_Kitaoka.pdf 2025年3月閲覧
13)Grogan M, Dispenzieri A. Heart Fail Rev. 2015; 20(2): 155-162.
14)Greve AM, et al. JAMA Cardiol. 2021; 6(3) 258-266.
15)Hanson JLS, et al. Circ Heart Fail. 2018; 11(2): e004000.
16)Hammarström P. et al. Proc Natl Acad Sci USA. 2002; 99(Suppl 4): 16427-16432.
17)Hornstrup LS. et al. Arterioscler Thromb Vasc Biol. 2013; 33(6): 1441-1447.