心疾患に潜むATTR-CM
監修:高知大学医学部 老年病・循環器内科学講座 教授 北岡裕章 先生
心疾患の適切な管理のために
動画要約
- トランスサイレチン型心アミロイドーシス(ATTR-CM)は、進行性かつ致死性の疾患であり、その進行を遅らせ、QOLを維持・改善するためには、早期診断・介入が重要となる。
- ATTR-CMの診断数は年々増加している一方、心不全をはじめとした心疾患のなかに、アミロイドーシスを原因とするものが一定数存在すると考えられ、合併する心疾患の管理に大きな影響を与えている可能性がある。
- 心疾患に潜むATTR-CMを疑うための指標として、Red-Flagがある。
- 心アミロイドーシス患者への99mTcピロリン酸シンチグラフィ導入の指標として、クリニカルシナリオ及びKumamoto Criteriaがある。
トランスサイレチン(TTR)は通常、四量体を形成していますが、様々な要因でTTR四量体が不安定化することが、ATTR-CM発症の根本原因です1,2)。不安定化を引き起こす要因として大きく2つのサブタイプにわけられます。加齢による変化を引き起こす野生型とTTR遺伝子変異による変化を引き起こす変異型にわけられ、それぞれ野生型トランスサイレチン型心アミロイドーシス(ATTRwt-CM)、変異型トランスサイレチン型心アミロイドーシス(ATTRv-CM)と呼ばれます1)。
[COI:著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]
2)Ruberg FL, et al. J Am Coll Cardiol. 2019; 73(22): 2872-2891.
[COI:著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]
「Red-Flag」とは日本語で「危険信号」を意味し、疾患を疑うために有用な症候のことを指します1)。
1) Red-Flag(ATTRwt-CM)2)
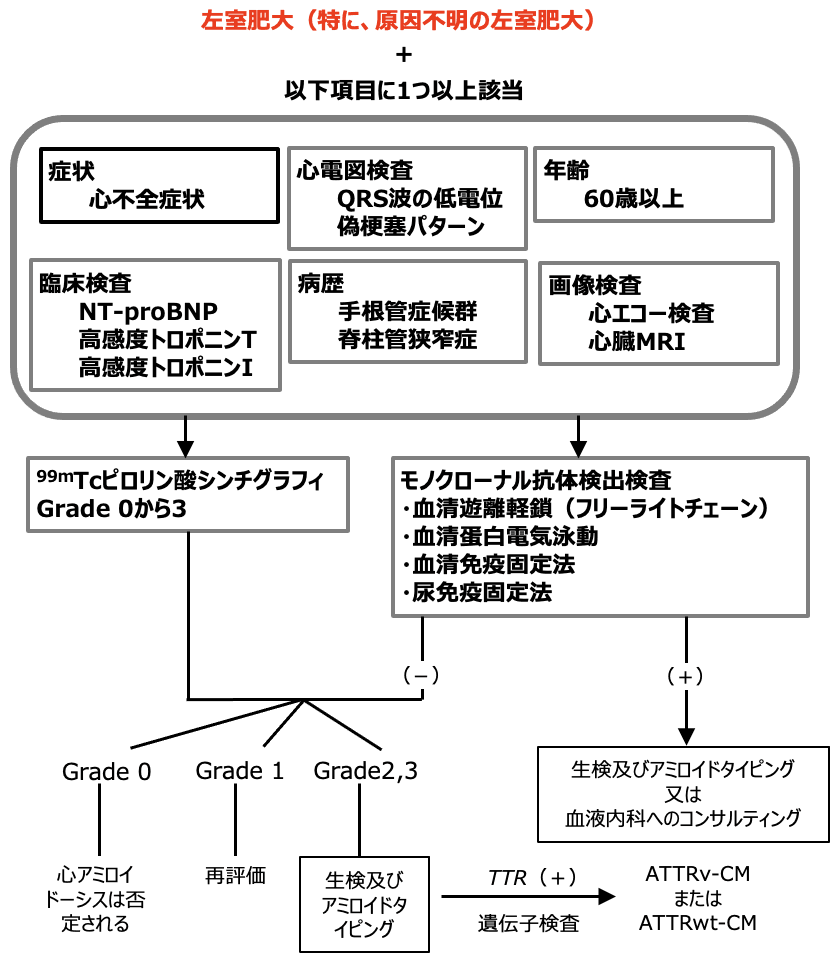
左室肥大(特に、原因不明の左室肥大)の症状をベースとして、以下に示す症状や年齢、病歴、各検査所見のうち1つ以上該当する項目があった場合、ATTRwt-CMを疑います。
ATTRwt-CMのRed-Flag症状及び徴候
Inomata T, et al. ESC Heart Fail. 2021; 8(4): 2647-2659.
2) Red-Flag(ATTRvアミロイドーシス)3)
糖尿病のない患者における亜急性又は慢性の神経障害(Yellow-Flag)を持ち、Red-Flagの徴候及び/又は症状のうち1つ以上がみられる場合、ATTRvアミロイドーシスを疑います。ATTRvアミロイドーシスでは眼症状が出る場合もあるため、追加で注意が必要となります。
ATTRvのRed-Flag症状及び微候
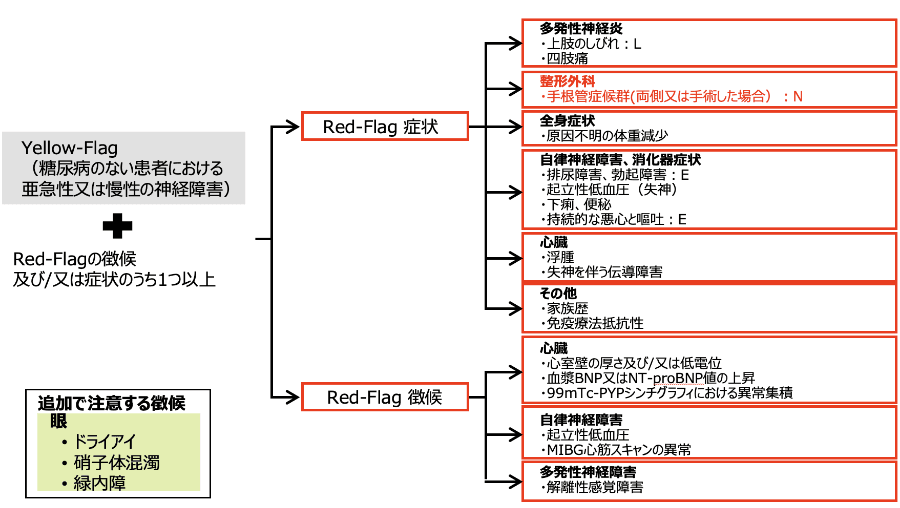
L:遅発性Val30Met変異、N:非Val30Met変異、E:早発性Val30Met変異
Sekijima Y, et al. Orphanet J Rare Dis. 2018; 13(1): 6.
[COI:著者のなかにはアレクシオンファーマ合同会社及びEidos Therapeutics,Inc.よりコンサルティング料等を受託している者が含まれる]
2)Inomata T, et al. ESC Heart Fail. 2021; 8(4): 2647-2659.
3)Sekijima Y, et al. Orphanet J Rare Dis. 2018; 13(1): 6.
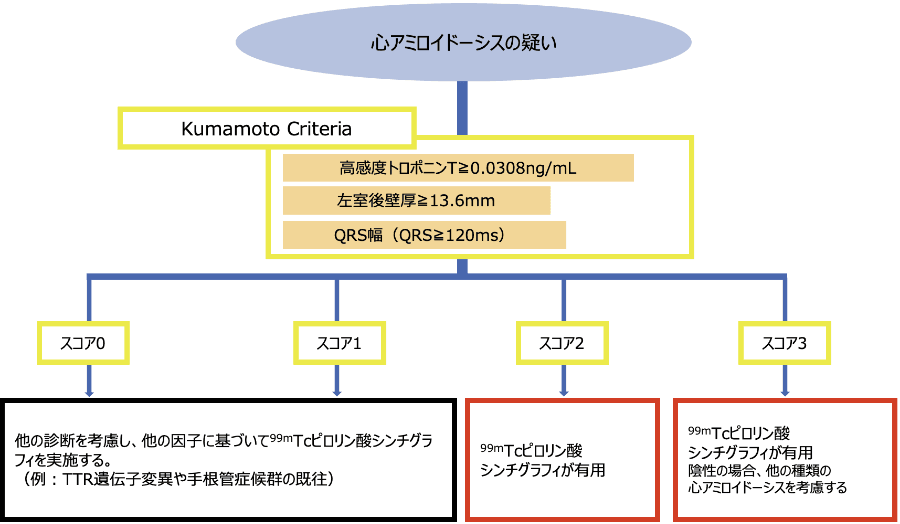
高齢者のATTR-CMを診断する際、99mTcピロリン酸シンチグラフィを実施する対象を効率的に選択するための基準です。低侵襲で広く使用されている検査方法を用います。
- 高感度トロポニンT≧0.0308ng/mL*1
- 左室後壁厚≧13.6mm
- QRS幅(QRS≧120ms)
の3つの因子について、それぞれスコアを1ずつ加算して用います。
*1:ATTR-CMの診断における高感度トロポニンTは保険適用外です。99mTcピロリン酸シンチグラフィを用いた新たな治療戦略
Marume K, et al. Circ J. 2019; 83(8): 1698-1708.
99mTcピロリン酸シンチグラフィ陽性患者の割合
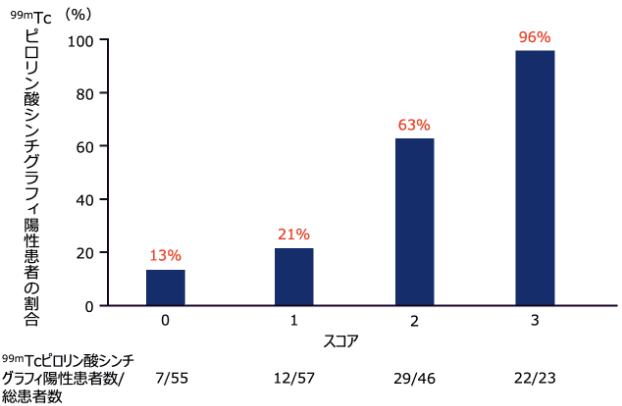
方法:Kumamoto Criteriaの3つの因子について、患者の状態に対して加算し、評価した。
リミテーション:第1に、本研究は単一施設研究であった。第2に、心筋生検は29%の患者にしか施行されていない。第3に、心アミロイドーシスに関するいくつかの指標を評価しなかった。心エコー検査における相対的心尖部温存は、心アミロイドーシスの顕著な特徴である(心アミロイドーシスと左室肥大の鑑別における感度93%、特異度82%)。しかし、熊本大学医学部附属病院では、心肥大のある患者全員に2次元スペックルトラッキング心エコー検査をルーチンに実施していなかったため、評価しなかった。最後に、ステップごとの選択プロセスの結果は、バイアスがかかる可能性があった。
Marume K, et al. Circ J. 2019; 83(8): 1698-1708.
スコアに応じた99mTcピロリン酸シンチグラフィの陽性率については、スコア0で13%、スコア1で21%、スコア2で63%、スコア3で96%であったと報告されています。
ATTR-CMの診断に至るまでのフローは、3段階に分けてみることができます。
1段階目では、心アミロイドーシスの可能性をスクリーニングします。心アミロイドーシスを念頭におくべき患者として原因不明の心不全が挙げられています。また、スクリーニング検査においても心エコー検査での心疾患所見や心不全のバイオマーカーでもあるトロポニンT等を調べることとされています。原因不明の心不全に注目し、これらの項目の組み合わせによって心アミロイドーシスを疑い、精査していくことが重要となります。
2段階目では、心アミロイドーシスの原因を非侵襲的な方法で病型分類していきます。ALアミロイドーシスの原因であるM蛋白の検出によるALアミロイドーシスの除外、シンチグラフィによる99mTcピロリン酸の心臓への集積程度により、ATTR-CMの「Probable診断」とすることが可能です。
3段階目では、侵襲的な病型分類(生検)と、ATTRアミロイドーシスの場合には遺伝子検査により確定診断(Definite診断)を行います。ALアミロイドーシスの場合は生検により、ATTRアミロイドーシスの場合は生検と、さらに遺伝子検査によってATTRv、ATTRwtを鑑別することで、Definite診断となります。
心アミロイドーシス診療アルゴリズム
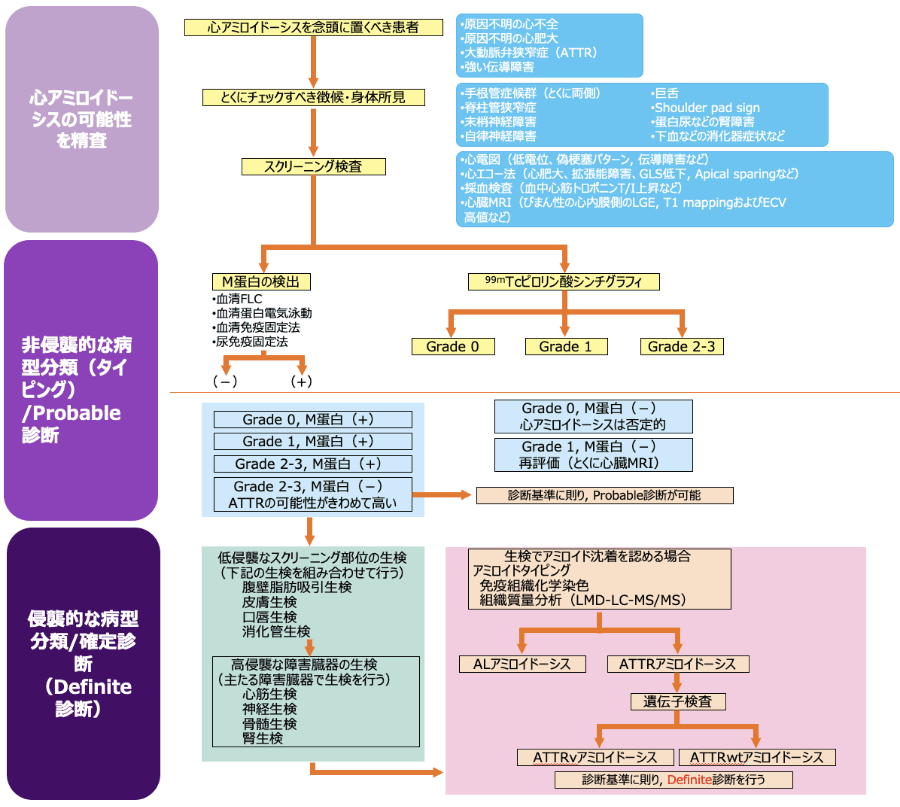
日本循環器学会.2020年版 心アミロイドーシス診療ガイドライン.
https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2020_Kitaoka.pdf 2025年3月閲覧
病期分類別の生存確率(海外データ)
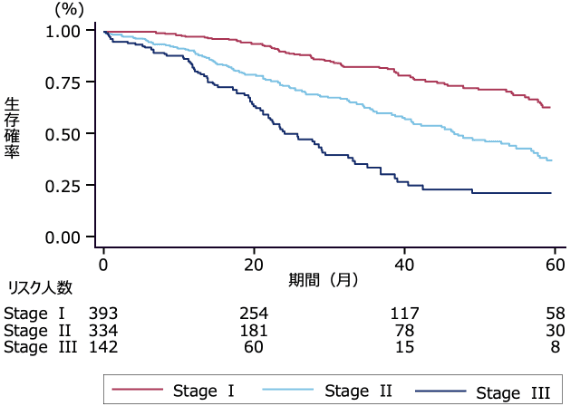
ATTR-CM診断時の重症度は、生存期間に影響を及ぼします。
NT-proBNPとeGFRを用いて、診断時のATTR-CMの病期分類を行い、生存率を解析した研究では、生存期間中央値がStage Iで69.2ヵ月、Stage IIで46.7ヵ月、Stage IIIで24.1ヵ月と、診断時の重症度が高いほど予後不良であったことが報告されています。一方、診断時の重症度が軽度の場合、つまりStage Iの場合は生存期間中央値が長いことも確認されています。したがって、軽症段階の早期にみつけ、適切に介入することが求められます。
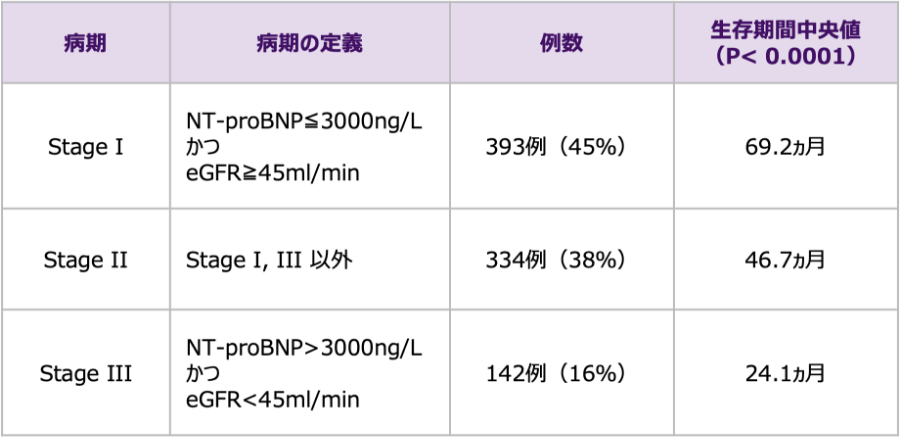
方法:NT-proBNPと推算糸球体濾過値(eGFR)に基づき、病期ステージを3つに層別化し、Kaplan-Meierにより生存率を解析した。
リミテーション:記載なし
Gillmore JD, et al. Eur Heart J. 2018; 39(30): 2799-2806.
近年、心疾患患者のなかに心アミロイドーシスを原因とする患者が一定数存在することを示唆する研究がいくつか発表されています。しかしながら、多様な合併症や認知度の低さ等から、診断の遅れが報告されています1)。
図で示す通り、左室駆出率の保たれた心不全(HFpEF)患者で左室壁の肥厚がある(12mm以上)患者を対象にした研究では、13%が99mTc-DPDシンチグラフィ陽性であったことが報告されています(海外データ)2)。
本研究の対象患者は、左室肥大があることや年齢60歳以上であったことが特徴です。
HFpEF及び左室壁の肥厚がある患者(海外データ)
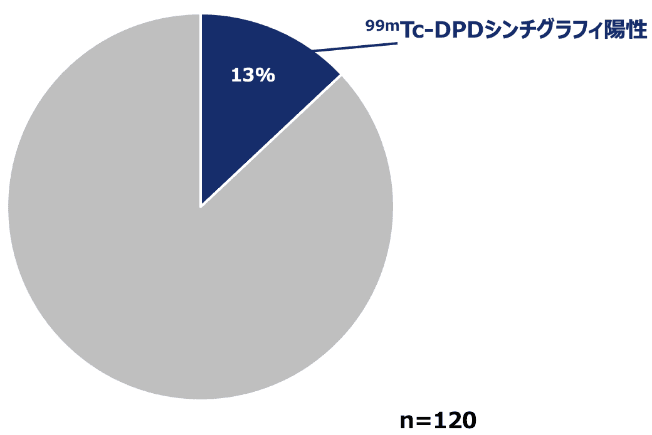
方法:入院中又は退院1週間後に99mTc-DPDシンチグラフィが施行され、シンチグラフィの結果を盲検化し、2人の医師が全患者の臨床記録を検討した。
リミテーション:第1に、組織学的確認は全例で得られていない。第2に、ESCによるHFpEFの定義を用いたが、ACCのHFpEFの定義を使用した場合、ATTRwtアミロイドーシス患者の数は変化した可能性がある。第3に、ATTRwtアミロイドーシスの検出に対するDPDスキャンの感度と特異度は不明であるため、ATTRwtアミロイドーシス患者の割合が過小評価される可能性がある。第4に、DPDシンチグラフィで陽性を示すことがあるApoA1アミロイドーシスを完全に除外することはできなかった。最後に、単一施設であることとプロトコールデザインによって制限されている。
González-López E, et al. Eur Heart J. 2015; 36(38): 2585-2594.より作図
本邦でも65歳以上のHFpEF患者を対象にした研究が行われ、14.2%が99mTcピロリン酸シンチグラフィ陽性*1であったことが報告されています3)。
HFpEF患者(国内データ)
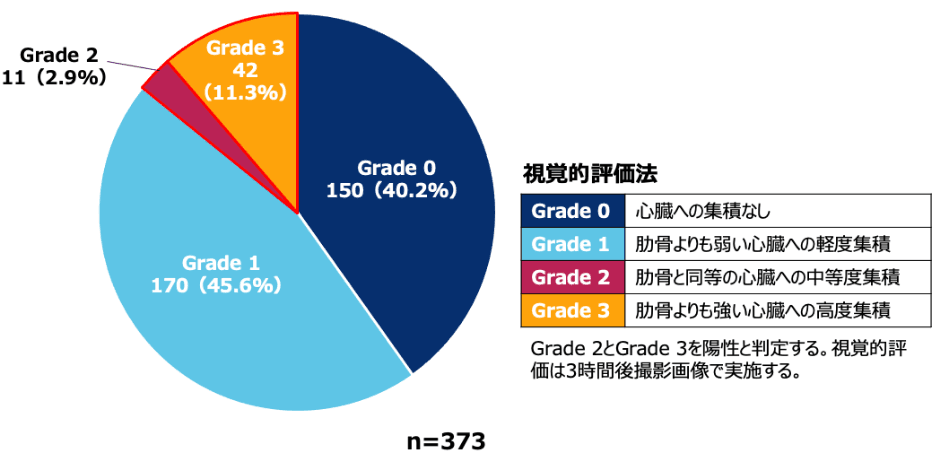
方法:入院中に99mTcピロリン酸シンチグラフィ検査を実施し、心臓の99mTcピロリン酸集積を視覚的評価法にしたがって評価した。
リミテーション:第1に、ATTR-CMがHFpEFと相乗的に死亡率に影響するかどうかは不明である。第2に、本研究の患者はHFpEFの検査前確率が高い紹介患者であったため、ATTR-CMの有病率には紹介バイアスがあるかもしれない。第3に、臨床的特徴及び心エコー検査に関する情報は、99mTcピロリン酸シンチグラフィの実施日とできる限り近い時期に入手したが、理想的には同日に得るべきである。第4に、ATTR-CMの遺伝子診断はどの症例でも行われなかった。第5に、アミロイド沈着の程度とピロリン酸の取り込みとの相関に関する利用可能なデータはない。最後に、本研究の結果はATTR-CM患者の一般集団を代表するものではない可能性がある。
Naito T, et al. ESC Heart Fail. 2023; 10(3): 1896-1906.
また、重度の大動脈弁狭窄症に対し、カテーテル治療を実施した患者のうち16%が99mTcピロリン酸シンチグラフィ陽性*1であったと報告されています4)(海外データ)。
*1:99mTcピロリン酸シンチグラフィはATTR-CMに対する高い診断能を有しているため5)、陽性の場合、アミロイドーシスが疑われる。大動脈弁狭窄症に対しカテーテル治療を実施した患者(海外データ)
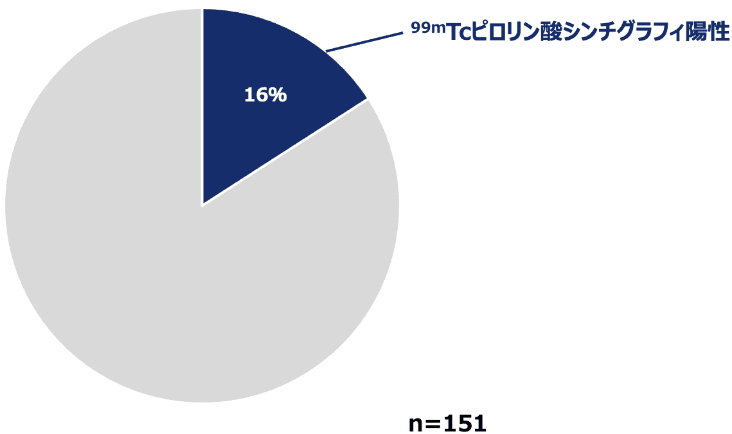
方法:TAVI施行後30日以内に99mTcピロリン酸シンチグラフィ検査を実施し、心臓の99mTcピロリン酸集積が視覚的評価法 ≧2、H/CL比 ≧1.5によりATTR-CMと評価した。
リミテーション:本研究は、紹介バイアスの影響を受けた。
また、ストレイン解析は心内壁の描出が十分な患者でのみ解析可能であったため、普遍的に行われたわけではない。さらに、すべての患者が99mTcピロリン酸シンチグラフィを受けたが、TAVIを受けている高齢者集団におけるリスクを考慮し、心臓生検は行われなかった。
本研究では、異常モノクローナル蛋白を認めたATTR-CM患者5人のうち、2人は正式な診断基準を満たし、単クローン性免疫グロブリン血症を有していたが、最終的に5人全員がALアミロイドーシスを正式に除外するための組織生検を受けないことを選択した。
Castaño A, et al. Eur Heart J. 2017; 38(38): 2879-2887.より作図
以上のことから、先生方が日常診療でよく診療する患者さんの中にATTR-CMの患者さんが隠れている場合があるため、原因不明の左室肥大があり、Red-Flagの徴候を有する方を診る際には、より慎重な評価が必要になります。
2)González-López E, et al. Eur Heart J. 2015; 36(38): 2585-2594.
3)Naito T, et al. ESC Heart Fail. 2023; 10(3): 1896-1906.
5)日本循環器学会.2020年版 心アミロイドーシス診療ガイドライン. https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2020_Kitaoka.pdf 2025年3月閲覧
心アミロイドーシスが関連する心疾患は、予後の悪化や、通常の治療が奏功しない場合があるとされています。
アミロイド由来の心不全は心筋リモデリングよりも、主に間質へのアミロイドの浸潤によって引き起こされるため、β遮断薬の使用は有益ではないとされ、ACE阻害薬やARBといった従来の心不全治療薬についても、忍容性が低く、症状の悪化を招くリスクがあるとされています1)。
また、心アミロイドーシス診療ガイドラインにおいても、ATTR-CMが合併する高度大動脈弁狭窄症への治療介入はリスクが高く、治療を行っても症状改善が乏しく予後不良と記載されています2)。
以上のことから、ATTR-CMが関連する心疾患は、予後や治療方針に影響を与える可能性があるため、適切な鑑別が必要です。
2)日本循環器学会.2020年版 心アミロイドーシス診療ガイドライン. https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2020_Kitaoka.pdf 2025年3月閲覧
