フォローアップの指標
監修:高知大学医学部 老年病・循環器内科学講座 教授 北岡裕章 先生
トランスサイレチン型心アミロイドーシス(ATTR-CM)患者の長期的なフォローアップにあたっては、血液検査や画像検査等の臨床検査データをはじめ、自覚症状や主観的な健康状態、問診や患者報告アウトカム(Patient
Reported Outcome:PRO)、入院イベントの有無等をモニタリングすることで、治療効果・病勢進行を評価することが重要です。
治療効果・病勢進行の評価に関する指標は、生存期間の延長をはじめ、入院回数の減少やQOL、予後バイオマーカーの安定又は改善等が有用と考えられています1)。
予後バイオマーカーとしては、血清トランスサイレチン(TTR)、NT-proBNP及び心筋トロポニン等が挙げられます。
現在のところ、治療効果の評価における画像診断(心エコー、磁気共鳴画像、陽電子放射断層撮影等)の役割は確立していません1)。
- 予後に関連するバイオマーカー(血清TTR、NT-proBNP及び心筋トロポニン)
- QOL(KCCQ-OS、症状の重症度)
- 機能的能力(6MWT)
- 合併する心疾患(増悪、入院)
[COI:著者のなかにはEidos Therapeutics,Inc.より研究助成金等を受領している者が含まれる]
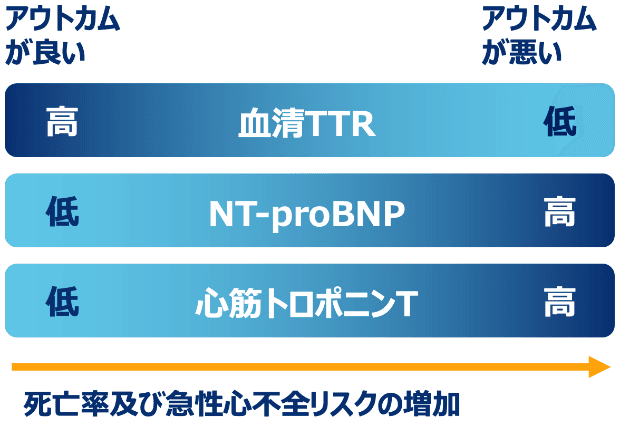
血清TTR、NT-proBNP及び心筋トロポニンTは、ATTR-CM患者の死亡率と急性心不全リスクの重要な予測バイオマーカーとして注目されています1-4)。
- 「心アミロイドーシス」に対して、保険診療として認められていません。
2)Law S, et al. Heart. 2022; 108(6): 474-478.
[COI:著者のなかにはEidos Therapeutics,Inc.の専門諮問委員会の者が含まれる]
4)Oghina S, et al. J Clin Med. 2021; 10(21): 4868.
5)Takashio S,et al. ESC Heart Fail. 2018; 5(1): 27-35.
血中TTR*:心不全の予防や生存期間の延長に関連する指標
- 「心アミロイドーシス」に対して、保険診療として認められていません。
加齢や遺伝子変異によってTTR四量体が不安定化することが、ATTR-CM発症の根本原因です。不安定化したTTR四量体が単量体へと解離し、アミロイド線維を形成することでATTR-CMを発症します。血中TTRレベルは、心不全の予防や生存期間の延長に関連する指標となる可能性があります。
血漿TTRレベルと心不全発症との関連を検討した研究で、血漿TTR低値群*、中間群*、高値群*で比較したところ、低値群では他2群より心不全の発症リスクが有意に高いことが報告されました(p
<0.001、Gray検定、海外データ)1)。
- 血漿TTRレベルが5パーセンタイル以下を低値群、5-95パーセンタイルを中間群、95パーセンタイル以上を高値群と定義している。
また、野⽣型ATTR-CM(ATTRwt-CM)患者の血清TTRレベルと生存率との関連について、血清TTRを低値群*、高値群*で比較した研究では、血清TTR 低値群は高値群と比較し生存期間が短かったことが報告されました(HR:2.3、95%CI:1.2~4.2、p=0.03、log-rank検定、海外データ)2)。
- 血清TTR18mg/dLを閾値として、18mg/dL以上を高値群、18mg/dL未満を低値群と定義している。
以上のことから、血中TTRレベルの低下は心不全の予防や生存期間の延長に悪影響を及ぼす可能性が高まることから、高い血中TTRレベルを維持することが重要になります。
累積発生率の関連(海外データ)1)
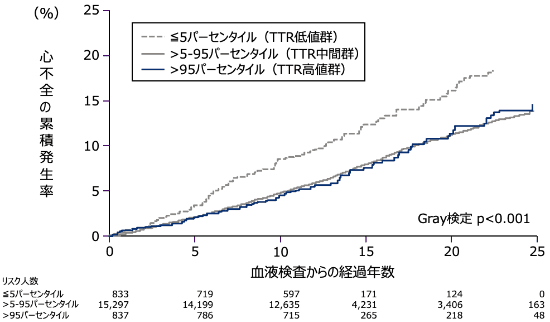
Reproduced with permission from [JAMA Cardiol. 2021. 6(3): 258-266].Copyright © 2021 American Medical Association. All rights reserved, including those for text and data mining, AI training, and similar technologies.
対象:2つのコホート研究に含まれたデンマークの一般母集団16,967例(Copenhagen General Population Study:9,582例、Copenhagen City Heart Study:7,385例)方法:全国市民登録システムを使用して自記式質問票、身体検査、及び血液検査からデータを取得し、TTRのパーセンタイルによって層別化された血液検査からの経過年数の関数としての心不全の累積発生率を算出した。
解析:層別化は血漿のTTR濃度で行われ、2つのコホート研究の集団毎に≦5パーセンタイル(TTR低値群)、>5-95パーセンタイル(TTR中間群)、>95パーセンタイル(TTR高値群)に分けられた*。血漿TTR濃度に最も関連するベースライン特性は95%CI正規化回帰係数によって特定され、ベースラインの血漿TTR濃度による心不全のハザード比はCox回帰によって計算した。また、競合イベントとして全死因死亡率を使用し、ノンパラメトリックなAalen-Johansen推定量を使用して、血液検査からの経過年数の関数として心不全の絶対確率を計算した。
リミテーション:高血圧や虚血性心疾患等の心不全の原因は特定できなかった。また、本研究ではサンプル数に限りがあるため2つのコホートにおいて異なるTTRの測定方法が使用され、白人のみを対象とした。
- Copenhagen General Population Study、 Copenhagen City Heart Studyについて、TTR低値群の濃度はそれぞれ7.0-19.0mg/dL、1.0-14.4mg/dL、TTR中間群の濃度はそれぞれ19.1-40.8mg/dL、14.5-38.0mg/dL、TTR高値群の濃度はそれぞれ40.9-77.7mg/dL、38.1-86.7mg/dLであった。
1)Greve AM, et al. JAMA Cardiol. 2021; 6(3): 258-266.
Kaplan-Meier解析(海外データ)2)
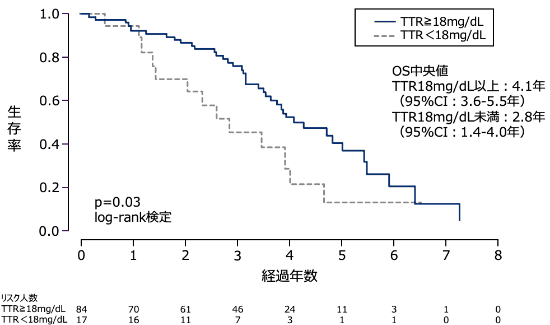
方法:追跡調査期間中に治療を受けなかった患者をベースラインのTTR閾値(18mg/dL)によって層別化し、生存率を比較した。
解析:追跡調査期間中に治療を受けなかった患者(n=101)を、ベースラインのTTR閾値18mg/dLによって層別化した。OS曲線はKaplan-Meier法で推定し、log-rank検定を用いて比較した。
リミテーション:比較的少人数の患者コホートでの検討のため、検出力は低かった。本研究では、心エコー、心臓MRI、核画像データ及びATTRwt-CM患者のモニタリングにおいて重要と考えられているNT-proBNP測定は行っていない。
2)Hanson JLS, et al. Circ Heart Fail. 2018; 11(2): e004000.
2)Hanson JLS, et al. Circ Heart Fail. 2018; 11(2): e004000.
NT-proBNP:心臓病変の検出に有用
NT-proBNPは、ストレスや圧力過負荷に反応して心臓から分泌され、心不全や心機能障害の悪化の指標となります。ATTR-CMにおいても、重要な指標の一つとして利用されています。
ΔNT-proBNPによって層別化された12ヵ月時点からの生存率を検討した研究において、低値群*は高値群*に比べて有意に生存確率が高かったという報告があります(p<0.001、多変量Cox回帰分析)1)。
- ΔNT-proBNPが2,000ng/L超を高値群、2,000ng/L以下を低値群と定義している。
本邦の心アミロイドーシス診療ガイドラインでは、「BNPおよびNT-proBNPは心不全のスクリーニングや診断、予後予測に汎用されるバイオマーカーである。心アミロイドーシス(とくにALアミロイドーシス)では心不全の重症度や血行動態に比してNT-proBNPの上昇が顕著であるとされている。ATTRvアミロイドーシスで心症状が出現する前からNT-proBNPが上昇しており、その上昇は心臓病変の検出に有用であったと報告されている。」と紹介されています2)。
Kaplan-Meier生存曲線(海外データ)1)
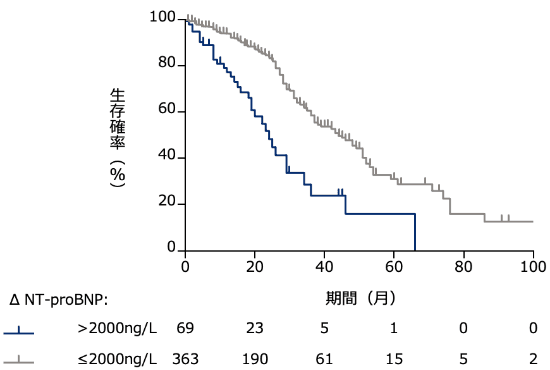
方法:診断から12ヵ月後のNT-proBNP濃度の変化(ΔNT-proBNP)によって層別化し、診断から12ヵ月の時点からの生存率を示した。
解析: ∆NT-proBNP >2,000ng/L又は≦2,000ng/Lによって層別化された12ヵ月の時点からの生存を、ランドマーク解析のKaplan-Meier生存曲線によって示した 。
リミテーション:本研究はレトロスペクティブなデザインで、追跡調査開始後1年以内に死亡した患者を除外しており、詳細な心エコー検査の変数は除外され、心臓磁気共鳴のデータが欠如していた。また、NT-proBNP濃度は他の因子と交絡する。さらに、本研究には疾患修飾療法を受けている患者は含まれない。
1)Law S, et al. Heart. 2022; 108(6): 474-478.
[COI:著者のなかにはEidos Therapeutics,Inc.の専門諮問委員会の者が含まれる]
[COI:著者のなかにはEidos Therapeutics,Inc.の専門諮問委員会の者が含まれる]
2)日本循環器学会.2020年版 心アミロイドーシス診療ガイドライン.
https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2020_Kitaoka.pdf 2025年3月閲覧
心筋トロポニン*:心筋障害のマーカー
- 「心アミロイドーシス」に対して、保険診療として認められていません。
心筋トロポニンの上昇は急性心筋梗塞の診断に用いられますが、心アミロイドーシスでも心筋トロポニンが持続的に上昇していることが報告され、Red-flagの1つとして挙げられています1)。
ATTRwt-CM患者を対象に生存(OS)に影響を及ぼす因子を検討した研究において、心筋トロポニンT高値群は、低値群と比較して生存期間が有意に短いと報告されました(p<0.001、log-rank検定)2)。
層別化された死亡率(海外データ)2)
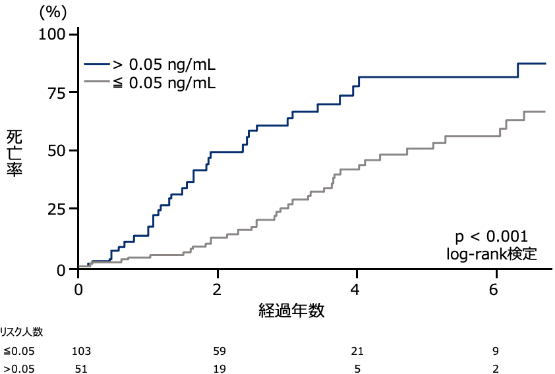
方法:心筋トロポニンTの値によって層別化し、死亡率を示した。
解析:0.05 ng/mLを閾値としてトロポニンTによって層別化された死亡率を、Kaplan-Meier法を用いて示し、log-rank検定を用いて比較した。ハザード比(HR)及び95%CIはCox比例ハザード回帰を用いて算出した。
リミテーション:本研究は、レトロスペクティブに行われ、一部の変数が不完全なデータであり、ニューヨーク心臓協会の機能分類が欠如していた。また、高血圧の病歴に関する詳細は入手できず、ジェノタイピング及び質量分析を受けていない患者が含まれる。
2)Grogan, M. et al. J Am Coll Cardiol. 2016; 68(10): 1014–1020.
https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2020_Kitaoka.pdf 2025年3月閲覧
2)Grogan, M. et al. J Am Coll Cardiol. 2016; 68(10): 1014–1020.
カンザスシティ心筋症質問票(KCCQ)は、身体機能、症状(頻度、重症度、安定性)、社会的機能、自己効力感、及びQOLを定量化する23項目からなる自記式質問票で、ATTR-CMの臨床試験でも評価項目として利用されています。(1)症状頻度と症状負担のドメインからなるTotal Symptom Score(TSS)、(2)身体的制限とTSSからなるClinical Summary Score(CSS)、(3)CSS、QOL、社会的制限のドメインを組み合わせたOverall Summary Score(OS)として要約されます。点数は0点から100点まであり、100点が最高点です。KCCQスコアが低いほど入院及び死亡のリスクが高いことが示されています1,2)。

1)Lane T, et al. Circulation. 2019; 140(1): 16-26.
TTRが単量体となりミスフォールドしたアミロイド線維は複数の器官系に影響を及ぼすため、様々な臨床的及び症候的特徴を示す可能性があります。すなわち、ATTR-CM患者では、典型的な病理学的症状として慢性かつ進行性の心不全が発現しますが、他の器官系にも影響が及ぶことがあります。
ATTR-CM患者が最も困ると感じる症状は、活動不耐性、運動不能、不眠症及び疲労でした(海外データ)3)。
ATTRアミロイドーシス患者が困ると感じる症状(器官系別、海外データ)3)
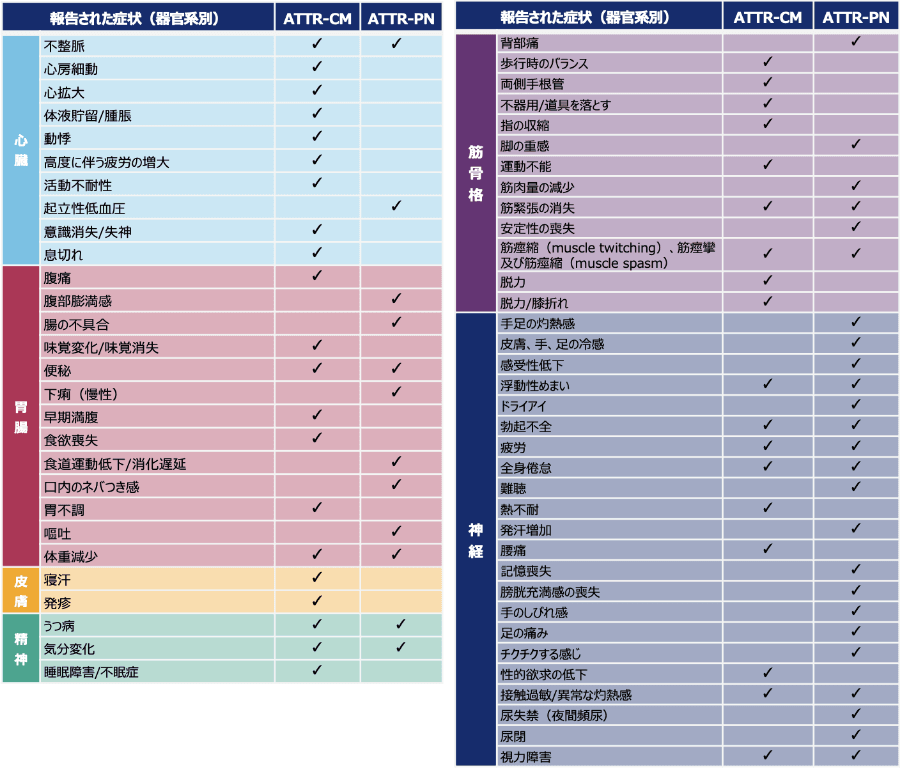
方法:フォーカスグループの実地経験を持つ心理学者が進行役をつとめるグループディスカッションを行い、患者及びその家族が身体の健康とQOLに影響を与えたATTRの症状をリストアップし、最も大きな影響を与えた3つを選んだ。
リミテーション:患者団体が参加者を募集し、プライバシー保護のために年齢などの人口統計は不明である。
3)Rintell D, et al. Orphanet J Rare Dis. 2021; 16(1): 70.
[COI:研究の資金はEidos Therapeutics,Inc.によって提供され、
著者のなかにはEidos Therapeutics,Inc.の社員が含まれる]
2)Butler J, et al. Circulation. 2022; 145(3): 184-193.
3)Rintell D, et al. Orphanet J Rare Dis. 2021; 16(1): 70.
[COI:研究の資金はEidos Therapeutics,Inc.によって提供され、著者のなかにはEidos Therapeutics,Inc.の社員が含まれる]
6分間歩行試験(6MWT)は、2002年に米国胸部医学会(American Thoracic Society; ATS)によってガイドラインが発表された、運動器具や技術者の高度な訓練を必要としない、実用的な簡易検査で、ATTR-CMの臨床試験でも評価項目として利用されています1)。

1)ATS Committee on Proficiency Standards for Clinical Pulmonary Function Laboratories. AM J Respir Crit Care Med. 2002; 166(1): 111-117.
2)Garcia-Pavia P, et al. Eur J Heart Fail. 2021; 23(4): 512-526.
[COI:著者のなかにはアレクシオンファーマ合同会社及びEidos Therapeutics,Inc.よりコンサルティング料等を受領している者が含まれる]
3)Solway S, et al. Chest. 2001; 119(1): 256-270.
2)Garcia-Pavia P, et al. Eur J Heart Fail. 2021; 23(4): 512-526.
[COI:著者のなかにはアレクシオンファーマ合同会社及びEidos Therapeutics,Inc.よりコンサルティング料等を受領している者が含まれる]
3)Solway S, et al. Chest. 2001; 119(1): 256-270.
ATTR-CM患者のフォローアップでは、入院、再入院の有無や回数が重要な指標となります。心不全増悪がある患者は増悪のない患者と比較し、全死亡率が有意に高かったことが報告されています(p<0.0001、時間依存性Cox回帰分析)1)。
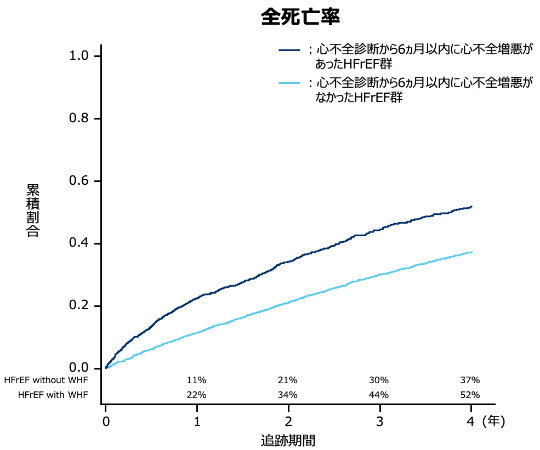
(95%CI:1.86-1.98;p<0.0001;時間依存性Cox回帰分析)
方法:初めにHFrEFと診断されてから6ヵ月後をランドマーク指標日とし、6ヵ月以内に心不全による入院またはED受診があった場合を“心不全増悪があったHFrEF群”(5,259例、52.8%)、なかった場合を“心不全増悪がなかったHFrEF群”(4,689例、47.2%)とした。それぞれの群において、HF診断6ヵ月後のランドマーク指標日から中央値4年間の全死亡と再入院の発生割合を後ろ向きに調査した。
解析:累積罹患率関数。ランドマーク指標日までの間に死亡した患者は除外した。両群の臨床転帰の比較には時間依存性Cox回帰分析を用いた。
リミテーション:行政の健康データを使用しており、診断・処置コードの正確性等のため、誤分類の可能性がある。また、 LVEFの状態に関するデータは、HFコホートのすべての患者については得られず、心エコーのデータが得られたサブセットについては紹介バイアスの可能性がある。血圧やNYHA分類等の臨床変数はデータベースから容易に入手できず、外来での静注利尿薬使用に関するデータが不足していた。また、データにはBNP等の検査変数を含む。処方薬のデータについて、HFrEFのために処方されたものかは確認できなかった。
1)Sepehrvand N, et al. J Card Fail 2022; 28(8): 1298-1308.
また、ATTR-CM患者の多くが併発するとされる心不全入院患者を対象とした研究では、1回目、2回目、3回目、4回目の入院後の生存期間の中央値は、それぞれ2.4年、1.4年、1.0年、0.6年と、入院回数の増加に伴い減少しました2)。
そのため、心不全を多く合併するATTR-CM診療においても、入院の抑制を目指した治療戦略が求められます。
生存期間中央値の関係(海外データ)2)
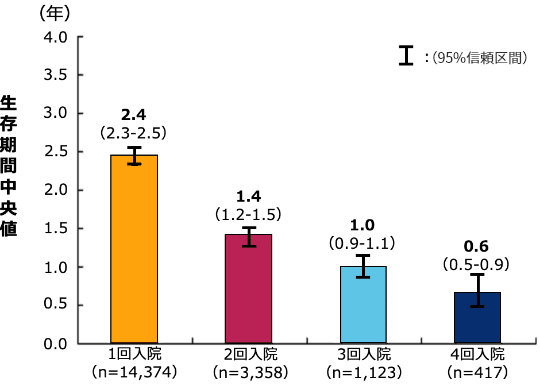
方法:医療利用データベースを用いて、2000年から2004年の間にブリティッシュ・コロンビア州の全住民のうち、心不全による初回入院を経験した患者コホートを同定した。患者の初回及びその後の各心不全入院後の生存期間を測定した。
リミテーション:第1に、今回のデータでは収縮機能障害と駆出率が保たれた心不全を区別することができなかった。第2に、 心不全の重症度の指標に関する臨床情報がないため、機能状態やQOLのような心不全の重症度を示す臨床指標で調整した後に、心不全の入院回数が独立して死亡率を予測するかどうかはわからない。
2)Setoguchi S, et al. Am Heart J. 2007; 154(2): 260-266.
2)Setoguchi S, et al. Am Heart J. 2007; 154(2): 260-266.
